لوسمی میلوئید حاد
لوسمی میلوئید حاد AML نوعی سرطان است که مغز استخوان تعداد زیادی سلول های خونی غیر طبیعی تولید می کند.
نکات کلیدی
- لوسمی میلوئیدی حاد بزرگسالان (AML) نوعی سرطان است که در آن مغز استخوان تعداد زیادی سلول های خونی غیرطبیعی می سازد.
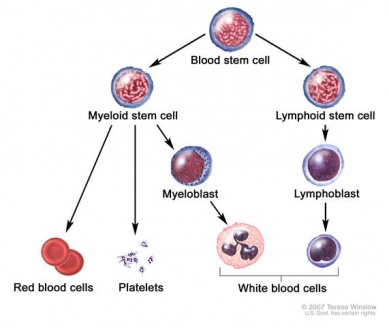
- لوسمی ممکن است روی گلبول های قرمز،سفید و پلاکت ها تاثیر بگذارد.
- انواع مختلفی از AML وجود دارد.
- سیگار کشیدن، درمان های قبلی با شیمی درمانی و قرارگیری در معرض تشعشع احتمال خطر ابتلا به میلوئید را افزایش می دهد.
- علائم و نشانه های AML شامل: تب، احساس خستگی و بی حالی و کبودی و خونریزی سریع است.
- از آزمایش خون و تست مغز استخوان برای تشخیص AML اسشتفاده می شود.
- بعد از تشخیص AML، آزمایش های تشخیصی جهت بررسی سرایت سرطان به دیگر اعضای بدن انجام می شود.
- عوامل خاصی بر پیش آگهی (احتمال بهبود) و روند درمان تاثیر می گذارند.
مقدمه:
لوسمی میلوئید حاد AML که با نام لوسمی حاد غیر لنفوسیتی (Acute Nonlymphocytic Leukemia -ANLL) نیز شناخته می شود، سرطان رده های سلول های خونی می باشد. این سرطان یک نئوپلاسم تهاجمی کلونال میلوئید می باشد که منجر به تجمع میلوبلاست ها (سلول های پیش ساز گلبول های سفید خونی که به صورت نابالغ می باشد) در مغز استخوان و/یا خون می شود.
رشد سریع این سلول های غیر نرمال در مغز استخوان باعث تداخل در تولید سلول های خونی طبیعی می گردد. لوسمی میلوئید حاد شایعترین لوسمی حاد بوده که بزرگسالان را تحت تاثیر قرار می دهد، و رخداد آن به همراه بالا رفتن سن افزایش می یابد، میانه سنی درگیری توسط لوسمی میلوئید حاد 70 سالگی بوده و رخداد آن پس از 60 سالگی به شدت افزایش می یابد.
شناسایی این بیماری توسط جایگزین شدن سلول های نرمال مغز استخوان توسط سلول های لوسمیک حاصل می شود، این جایگزینی باعث کاهش در گلبول های قرمز خون ، پلاکت ها و گلبول های سالم می گردد.
این علائم شامل، خستگی ، تنگی نفس، رنگ پریدگی(که همه از نتایج کاهش در تعداد گلبول های قرمز یا کم خونی می باشد)، ایجاد ساده خونریزی ها، کبودی ها(به علت کاهش در تعداد پلاکت های خونی) و افزایش خطر ایجاد عفونت می باشد. فقدان گلبول های سفید خون باعث می شود که بیماران به عفونت ها حساس شوند، با وجود اینکه سلول های لوسمیک خودشان از پیش سازهای گلبول های سفید حاصل شده اند، ولی ظرفیت درگیری با عفونت ها را ندارند.
معمولاً اولین علائم این بیماری مبهم می باشند، و ممکن است شبیه علائم بیماری انفلوآنزا باشند. بزرگ شدن طحال ممکن است در این بیماران رخ دهد، اما معمولاً خفیف و بدون علامت خواهد بود. برخلاف لوسمی لمفوبلاستیک حاد، تورم گره های لنفی در این بیماری نادر می باشد. پوست در ده درصد از بیماران درگیر می شود، برخی بیماران با لوسمی میلوئید حاد ممکن است به علت نفوذ سلول های لوسمیک به داخل بافت لثه دچار تورم لثه شوند.
در موارد کمی ممکن است اولین علامت این بیماری ایجاد و رشد یک جسم لوسمیک جامد یا تومور خارج از مغز استخوان باشد، که کلروما(chloroma) نامیده می شود. گاهی، برخی از افراد مبتلا به بیماری هیچ علائمی از خود بروز نمی دهند، و لوسمی ممکن است بصورت تصادفی در حین آزمایش های خون روتین شناسایی شود. چند عامل خطر برای ایجاد لوسمی میلوئید حاد تاکنون شناسایی شده است که شامل مواردی مثل اختلالات خونی، در معرض قرار گیری توسط عوامل شیمیایی، اشعه های یونیزان و عوامل ژنتیکی می باشد.
شروع تشخیص قطعی این بیماری از یافتن یک سرنخ از نتیجه غیرمعمول در بررسی خون کامل می باشد. در حالیکه افزایش گلبول های سفید غیر معمولی یکی از یافته های شایع می باشد، بلاست های لوسمیک تنها در برخی موارد شناسایی می شوند، این بیماری می تواند با کاهش در تعداد پلاکت ها، گلبول های قرمز خون، حتی با کاهش در تعداد گلبول های سفید (لوکوپنی) همراه باشد.
تشخیص احتمالی لوسمی میلوئید حاد می تواند از طریق بررسی گستره های خونی محیطی، همراه با وجود بلاست های لوسمیک در گردش خون ایجاد شود، تشخیص قطعی معمولاً به بیوپسی های مغز استخوان احتیاج دارد.
خون یا مغز استخوان از طریق میکروسکوپ نوری و فلوسیتومتری، برای تشخیص وجود لوسمی مورد بررسی قرار می گیرند. این روش ها همچنین، برای تمایز لوسمی میلوئید حاد از سایر انواع لوسمی (برای مثال لوسمی لمفوبلاستیک حاد)، و برای دسته بندی انواع بیماری مورد استفاده قرار می گیرند. روش های روتین سیتوژنتیک یا هیبریداسیون فلورسانس درجا (FISH) بر روی نمونه مغز استخوان یا خون برای بررسی ناهنجاری های کروموزومی مورد استفاده قرار می گیرند.
همچنین مطالعات ژنتیک مولکولی ممکن است برای بررسی جهش های خاص در ژن هایی مثل FLT3، نوکلئوپلاسم و KIT مورد انجام قرار گیرد. در برخی از موارد شناسایی و دسته بندی لوسمی میلوئید حاد چالش برانگیز می باشد، و می باید توسط هماتولوژیست ها یا هماتوپاتولوژیست های مجرب انجام گیرد.
فراوانی
تعداد موارد جدید از لوسمی میلوئید حاد 4 در هر 100000 نفر در سال می باشد. تعداد مرگ و میر ناشی از این بیماری 2/8 در هر 100000 نفر در سال می باشد.
تغییرات ژنتیکی
امروزه با استفاده از تکنیک های تشخیصی نوین تعداد جهش هایی که در بیماری لوسمی میلوئید حاد در حال تشخیص می باشند درحال گسترش می باشد. برخی از این ژن ها در ادامه توضیح داده می شوند.
BAG1 این ژن یک پروتئین چند عملکردی را کد می کند که در مسیرهای مختلفی در سلول دخیل است که همگی با بقای سلول در ارتباط می باشند. گزارش شده است که بیان آن در سرطان های مختلفی غیر منظم می شود. یکی از این سرطان ها لوسمی میلوئید حاد می باشد. این ژن باعث کاهش بیان ژن های BCL2، BCLXL ، MCL1 و فسفو- ERK1/2 می شود. تمام این پروتئین ها قادر به حفظ حالت لوسمی می باشند. اما این روند هیچ اثری بر روی کاهش بیان پروتئین پیش آپوپتوزی BAX نداشته است.
MDM2؛ ژن TP53 یک ژن سرکوبگر تومور است که در نیمی از موارد سرطان های جامد جهش یافته می یابد. در برخی از بدخیمی های خونی نیز جهش های TP53 با فراوانی نسبتاً پائینی مشاهده می شود، و بسیاری از این تومورها نوع وحشی را بیان می کنند. به هر صورت سلول های لوسمیک اختلالاتی را در پروتئین های تنظیم کننده مسیر TP53 نشان می دهند که یکی از موارد شایع افزایش بیان ژن MDM2 می باشد، که با شیوع بالا باعث غیر فعال شدن مسیر TP53 می شود. مشخص شده است فعال کردن عملکرد ضد توموری TP53 از طریق جلوگیری از اثر کرد مهاری MDM2 به عنوان یک استراتژی موثر در درمان سرطان ها شناخته شده است.
BCL2؛ نقایص در مسیر آپوپتوتیک می تواند باعث ارتقاء بقاء سلول های سرطانی و همچنین باعث بالا رفتن مقاومت نسبت به داروهای آنتی نئوپلاستیک شود. یکی از مسیرهایی که برای درمان های آنتی نئوپلاستیک هدف گیری می شود، مسیر آنتی آپوپتوتیک پروتئین های خانواده لنفومای Bسل2 (Bcl-2) ، Bcl–XL، Bcl–w، Mcl–1، Bfl1/A-1 و Bcl-B می باشد. افزایش بیان اعضای خانواده Bcl-2 با مقاومت به شیمی درمانی در برخی از سرطان های انسانی همراه می باشد.
Survivin این ژن یکی از اعضای خانواده IAP می باشد. و در تنظیم چرخه و مرگ سلولی نقش دارد، که در هر دو مورد نقشش به بقای سلول های سرطانی می انجامد. بیان این ژن توسط p53 سرکوب شده و توسط برخی انکوژن ها افزایش می یابد. بیان افزایش یافته این ژن در تعدادی از بدخیمی های خونی شامل لوسمی میلوئید حاد مشاهده شده است. همچنین سطح بیان این ژن با میزان مقاومت به شیمی درمانی ارتباط مستقیم دارد. سلول های CD34+،CD38- که پیش سازها و سلول های بنیادین سلول های لوسمیک میلوئید حاد می باشند سطوح بالاتری از بیان این ژن را نشان می دهند، این یافته پیشنهاد کننده این است که این ژن در بقا، و خودبازسازی سلول های بنیادی لوسمیک میلوئید حاد نقش دارد.
XIAP یکی از اعضای دیگر خانواده IAP می باشد. این ژن توجه ویژه ای را به عنوان هدف درمانی به خود اختصاص داده است به این دلیل که هم مسیر داخلی و هم مسیر خارجی آپوپتوز را مهار می کند. علاوه بر این بیان این ژن در لوسمی ها به شدت بالا می رود. همچنین افزایش بیان آن با مقاومت به شیمی درمانی همراه می باشد. این ژن در لوسمی میلوئید حاد افزایش بیان دارد این مشاهده از عملکرد افزایش دهنده بقای این ژن، در لوسمی حمایت می کند.
CEBPA کد کننده پروتئینی است به نام پروتئین آلفای متصل شونده به افزایش دهنده CCAAT (CCAAT/enhancer-binding protein alpha) می باشد. این پروتئین یک فاکتور رونویسی می باشد که تنظیم کننده بیان ژن های مختلفی می باشد. تصور بر این است که این ژن یک سرکوبگر تومور می باشد. جهش های ایجاد شده در این ژن باعث ایجاد یک پروتئین کوتاهتر می شود. جهش در این ژن باعث ایجاد نوعی لوسمی میلوئید حاد به نام لوسمی میلوئید خانوادگی می شود.
الگوی توارث
لوسمی میلوئید حاد خانوادگی با جهش در ژن CEBPA با الگوی توارث اتوزومی غالب به ارث می رسد. اغلب افرادی که در سلول های خود جهش در یکی از آلل های این ژن را به ارث برده اند همچنین در طول زندگی جهش های سوماتیک در سلول های لوسمی این افراد باعث می شود آلل دوم نیز دچار جهش بشود و عملکرد خود را از دست بدهد. به همین دلیل الگوی توارث این بیماری به صورت اتوزوم غالب خواهد بود. به این روند دو مرحله ای جهش یابی فرضیه ی دو ضربه ای نادسون گفته می شود.
نام های دیگر
لوسمی حاد غیر لنفوسیتی
لوسمی میلوبلاستیک